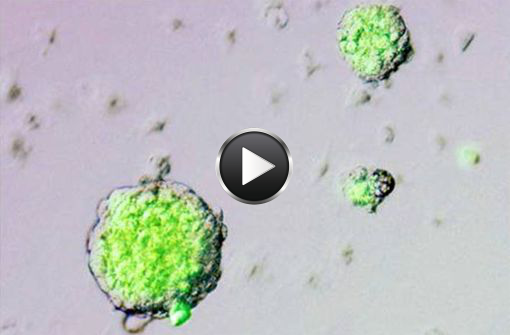
Cellules STAP photographiées par Haruko Obokota et son équipe (© Riken center for developmental biology).
Un bain d'acide transforme des globules blancs de souris en cellules "STAP"
Haruko Obokota, biologiste au Centre RIKEN de biologie du développement (Kobé, Japon), a remarqué que lorsque des cellules étaient "compressées" dans un mini-tube à essai, leur taille se réduisait et devenait similaire à celle d'une cellule souche.
Cette expérience lui a fait poser l'hypothèse qu'un simple "stress" cellulaire (compression physique, exposition à une toxine, température élevée, bain d'acide, etc.) pouvait transformer une cellule mature en cellule pluripotente.
Pour convaincre ses pairs de la nature pluripotente des cellules obtenues, Haruko Obokota a filmé l'immersion de globules blancs (lymphocytes T) matures de souriceaux dans une solution légèrement acide (pH de 5,7), à 37 °C, puis cultivés pendant une semaine.
Ce simple bain de 30 minutes a permis la transformation d'une partie des lymphocytes T survivants en cellules indifférenciées, appelées STAP (pour "stimulus-triggered acquisition of pluripotency", acquisition de pluripotence déclenchée par un stimulus). Dans la vidéo ci-dessous, 2 lymphocytes T se transforment en cellules STAP. Ils expriment alors un gène de pluripotence et deviennent verts (via un marqueur phosphorescent) :
Démonstration de la capacité de transformation des cellules STAP
L'expérience filmée ci-dessus montre qu'effectivement, un stress physique peut transformer les cellules survivantes à ce stress : 25 % des lymphocytes ont survécu, et 30 % de ces 25 % se sont transformés en cellules STAP.
Haruko Obokota et ses collègues ont ensuite réussi à démontrer que ces cellules STAP ont les mêmes propriétés que les cellules souches embryonnaires, adultes ou iPS. Pour cela, ils en ont injecté dans un blastocyte (embryon ne comportant que quelques cellules, tout jeune donc) en utilisant la technique de la complémentation tétraploïde (bien expliquée dans cet article de Tom Roud). Cette technique particulière permet le développement de l'embryon uniquement à partir des cellules pluripotentes injectées.
Résultat, un embryon de souris s'est développé normalement, composé à 100 % de cellules STAP (phosphorescentes au microscope électronique). Ces cellules se sont donc différenciées en cellules cutanées, pulmonaires, cérébrales, cardiaques (cf. le cœur battant ci-dessous), etc. :
Les cellules STAP possèdent des propriétés supplémentaires par rapport aux autres cellules pluripotentes
Non seulement les cellules STAP sont pluripotentes, mais elles peuvent, de plus, se différencier en cellules placentaires, ce que ni les cellules souches embryonnaires ni les cellules iPS (cellules pluripotentes induites, cf. notre article de juillet 2013) ne peuvent faire.
En théorie, l'injection de telles cellules dans un blastocyte pourrait donc créer un embryon capable de s'implanter dans l'utérus de la mère (animale, voire humaine) et de générer un placenta.
En conclusion : une "extraordinaire pluripotence" qui ouvre "de nouvelles possibilités"
 A condition d'être confirmée chez l'homme et en l'absence de multiplication anarchique secondaire des cellules modifiées, cette découverte étonnante pourrait permettre de faciliter la production de cellules pluripotentes performantes et donc, peut-être, accélérer la recherche sur les utilisations potentielles de ces cellules.
A condition d'être confirmée chez l'homme et en l'absence de multiplication anarchique secondaire des cellules modifiées, cette découverte étonnante pourrait permettre de faciliter la production de cellules pluripotentes performantes et donc, peut-être, accélérer la recherche sur les utilisations potentielles de ces cellules.Pour Haruko Obokota, "c'est excitant de penser aux nouvelles possibilités ouvertes par ces résultats, non seulement dans des domaines comme celui de la médecine régénérative, mais peut-être aussi pour l'étude du vieillissement cellulaire et du développement des cancers. Mais le plus grand défi pour moi à l'avenir sera d'approfondir davantage les mécanismes sous-jacents, afin que nous puissions mieux comprendre comment des cellules différenciées peuvent se transformer en un tel état extraordinairement pluripotent".
Jean-Philippe Rivière
Sources et ressources supplémentaires :
- "Stimulus-triggered fate conversion of somatic cells into pluripotency", Obokota H et coll., Nature, 20 janvier 2014
- "STAP cells overturn the pluripotency paradigm", communiqué du Centre RIKEN de biologie du développement (Riken center for developmental biology), janvier 2013
- "Pluripotent cells generated by STAP/ ???????3???", vidéo de la transformation des lymphocytes T en cellules STAP, chaîne YouTube du Centre Riken, 29 janvier 2014
- "STAP cells contribute to embryonic development/ 100%????", vidéo de l'embryon de souris composé à 100 % de cellules STAP, chaîne YouTube du Centre Riken, 29 janvier 2014
- "Cellules souches, les mères de toutes les cellules", ancien site de Tom Roud, 2008
- "Young Japanese scientist leads her team to major stem cell discovery", Mainichi, Japon, 30 janvier 2014
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.