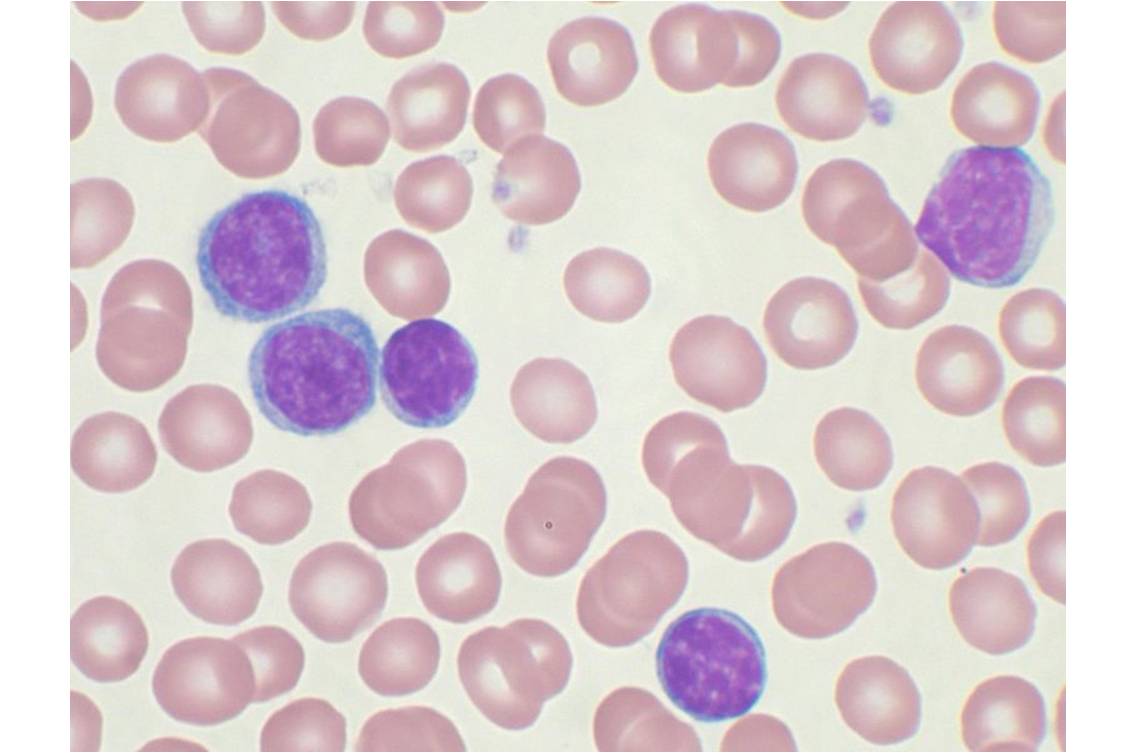
Lymphocytes B (cytoplasme bleu et noyau violet) lors d'une LLC, observés sur sang périphérique (@ Mary Ann Thompson, Wikimedia).
L'IBRUTINIB 140 mg gélule a reçu un avis favorable à la demande d'ATU (autorisation temporaire d'utilisation) de cohorte, déposée par le laboratoire Janssen-Cilag auprès de l'Agence nationale de sécurité du médicament et des produits de santé (ANSM), dans les indications suivantes :
- traitement des patients adultes atteints d'un lymphome à cellules du manteau (LCM) en rechute ou réfractaire ;
- traitement des patients adultes atteints d'une leucémie lymphoïde chronique (LLC) ou d'un lymphome lymphocytique (LL) en rechute ou réfractaire.
"Les patients atteints d'un lymphome à cellules du manteau ou d'une leucémie lymphoïde chronique, en rechute ou réfractaires, vont ainsi pouvoir accéder rapidement à ce traitement qui représente une avancée par rapport à l'existant" se félicite l'ANSM qui précise que le produit sera disponible dans les prochaines semaines. Pour les patients qui ne pourraient pas attendre cette échéance, des autorisations nominatives pourront être délivrées par l'ANSM selon les critères établis dans le cadre de l'ATU de cohorte.
Une procédure d'autorisation de mise sur le marché (AMM) centralisée est en cours au niveau européen. L'IBRUTINIB 140 mg gélule dispose depuis novembre 2013 d'une AMM aux Etats-Unis.
A propos de l'ibrutinib
L'ibrutinib est un inhibiteur covalent de la tyrosine kinase de Bruton.
Les études précliniques ont montré que l'ibrutinib inhibe efficacement la prolifération et la survie in vivo des cellules B malignes, ainsi que la migration cellulaire et l'adhésion au substrat in vitro.
Les études précliniques ont montré que l'ibrutinib inhibe efficacement la prolifération et la survie in vivo des cellules B malignes, ainsi que la migration cellulaire et l'adhésion au substrat in vitro.
En pratique
Le traitement par ibrutinib doit être instauré et surveillé par un médecin expérimenté dans l'utilisation des médicaments anticancéreux.
Ibrutinib doit être poursuivi jusqu'à progression de la maladie ou intolérance du patient.
Ibrutinib doit être poursuivi jusqu'à progression de la maladie ou intolérance du patient.
La posologie recommandée d'ibrutinib est :
- dans le traitement du lymphome à cellules du manteau : de 560 mg (4 gélules de 140 mg) 1 fois par jour ;
- dans le traitement de la leucémie lymphoïde chronique et du lymphome lymphocytique : de 420 mg (3 gélules de 140 mg) 1 fois par jour.
Des examens doivent être réalisés avant d'instaurer le traitement (numération formule sanguine, examens sériques et test de grossesse).
IBRUTINIB 140 mg gélule doit être administré par voie orale, 1 fois par jour avec un grand verre d'eau, environ une demi-heure avant ou 2 heures après un repas, si possible à la même heure chaque jour.
Les gélules doivent être avalées entières avec de l'eau, sans être ouvertes, cassées ni mâchées.
Ce médicament ne doit pas être pris avec du jus de pamplemousse.
Les gélules doivent être avalées entières avec de l'eau, sans être ouvertes, cassées ni mâchées.
Ce médicament ne doit pas être pris avec du jus de pamplemousse.
Sources et ressources complémentaires
L'ANSM notifie l'ATU de cohorte pour l'Ibrutinib dans deux indications - Point d'information (ANSM, 17 février 2014)
Résumé des caractéristiques du produit et notice d'information (ANSM, février 2014)
Sources
Pour recevoir gratuitement toute lãactualitûˋ par mail Je m'abonne !

 2 minutes
2 minutes Ajouter un commentaire
Ajouter un commentaire






Commentaires
Cliquez ici pour revenir à l'accueil.