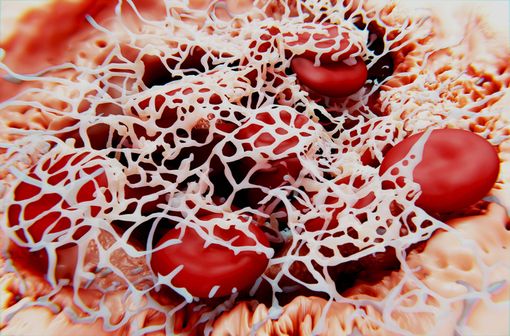
Représentation en 3D d'un caillot sanguin, où les globules rouges sont enserrés dans un maillage de fibrine (illustration).
Résumé :
THERASOLV poudre pour solution injectable pour perfusion est une nouvelle spécialité, formulée à base d'urokinase, indiquée dans la lyse intravasculaire des caillots sanguins associés à 4 situations (thrombose des cathéters veineux, thrombose veineuse profonde, embolie pulmonaire, artériopathie périphérique oblitérante).
THERASOLV est disponible sous 3 dosages :
Après reconstitution, la solution injectable THERASOLV doit être administrée en perfusion intraveineuse (IV), en injection intra-artérielle ou en instillation locale.
Réservé à l'usage hospitalier, THERASOLV est agréé aux collectivités, avec une prise en charge limitée à la lyse des caillots sanguins associés à une thrombose des cathéters veineux ou à une artériopathie périphérique oblitérante aiguë.
Un nouveau médicament antithrombotique à base d'urokinase est mis à disposition en France, à l'hôpital : THERASOLV poudre pour solution injectable pour perfusion.THERASOLV poudre pour solution injectable pour perfusion est une nouvelle spécialité, formulée à base d'urokinase, indiquée dans la lyse intravasculaire des caillots sanguins associés à 4 situations (thrombose des cathéters veineux, thrombose veineuse profonde, embolie pulmonaire, artériopathie périphérique oblitérante).
THERASOLV est disponible sous 3 dosages :
- 100 000 UI par flacon,
- 250 000 UI par flacon,
- 500 000 uI par flacon.
Après reconstitution, la solution injectable THERASOLV doit être administrée en perfusion intraveineuse (IV), en injection intra-artérielle ou en instillation locale.
Réservé à l'usage hospitalier, THERASOLV est agréé aux collectivités, avec une prise en charge limitée à la lyse des caillots sanguins associés à une thrombose des cathéters veineux ou à une artériopathie périphérique oblitérante aiguë.
THERASOLV est indiqué pour la lyse intravasculaire des caillots sanguins dans 4 situations :
- thrombose des cathéters veineux centraux et périphériques ;
- thrombose veineuse profonde proximale aiguë étendue ;
- embolie pulmonaire aiguë massive ;
- artériopathie périphérique oblitérante aiguë avec menace d'ischémie d'un membre.
Son principe actif, l'urokinase, est une forme hautement purifiée d'urokinase humaine naturelle extraite de l'urine. L'urokinase provoque une diminution dose-dépendante des taux de plasminogène et de fibrinogène et une présence accrue des produits de dégradation de la fibrine et du fibrinogène, qui exercent un effet anticoagulant et potentialisent l'effet de l'héparine.
Ces effets persistent pendant 12 à 24 heures après la fin de la perfusion d'urokinase.
Une gamme réservée à l'usage hospitalier
La gamme THERASOLV est réservée exclusivement à un usage hospitalier.
Elle comporte de 3 dosages différents d'urokinase :
Évaluation médico-économique de THERASOLV : des conclusions différentes en fonction de la situation
L'autorisation de mise sur le marché (AMM) a été octroyée sur la base d'un usage médical bien établi et repose essentiellement sur une revue de la littérature scientifique.
La prise en charge dans le cadre de l'agrément aux collectivités de THERASOLV a fait l'objet d'un avis de la Commission de la Transparence (CT) publié le 5 février 2020.
SMR important dans le cas de la thrombose des cathéters
La demande de prise en charge déposée par le laboratoire concernait uniquement la lyse des caillots sanguins en cas de thrombose des cathéters veineux centraux et périphériques.
Dans cette indication, la CT a attribué à THERASOLV un service médical rendu (SMR) important ; elle considère THERASOLV comme un traitement de première intention dans la stratégie thérapeutique, au même titre que les autres agents thrombolytiques actuellement disponibles dans cette indication.
SMR faible ou insuffisant dans les autres situations
Malgré la demande restreinte déposée par le laboratoire, la CT a analysé les autres situations prévues par l'AMM :
- artériopathie périphérique oblitérante aiguë avec menace d'ischémie d'un membre : SMR faible. THERASOLV peut être considéré comme un traitement de première intention dans la prise en charge de l'ischémie artérielle aiguë uniquement en l'absence de déficit neurologique ;
- thrombose veineuse profonde proximale aiguë étendue et embolie pulmonaire aiguë massive : SMR insuffisant, pas de place dans la stratégie thérapeutique.
THERASOLV en pratique
Selon l'indication, THERASOLV doit être administré en perfusion intraveineuse (IV), en injection intra-artérielle ou en instillation locale.
Il ne doit pas être injecté par voie sous-cutanée ou intramusculaire.
Reconstitution avant utilisation
THERASOLV se présente en poudre pour solution injectable.
La solution injectable doit être reconstituée avant utilisation, par dissolution de la poudre dans un volume approprié de solution injectable de chlorure de sodium à 9 mg/mL (NaCl 0,9 %).
Le solvant n'est pas fourni dans le conditionnement de THERASOLV.
Posologie et mode d'administration
La dose de THERASOLV à injecter ainsi que le mode d'administration sont définies en fonction de l'indication, de l'état clinique du patient et de la réponse au traitement (cf. monographies VIDAL) :
- situation de thrombose des cathéters veineux centraux et périphériques : la solution est administrée dans la lumière du cathéter et laissée en place (procédure verrou) pendant 20 à 60 minutes. Le lysat doit ensuite être aspiré ;
- situation de thrombose veineuse profonde proximale aiguë étendue : la solution est administrée en perfusion dans une veine périphérique ;
- situation d'embolie pulmonaire aiguë massive : la solution est administrée en perfusion dans une veine périphérique ou en bolus dans l'artère pulmonaire ;
- situation d'artériopathie périphérique oblitérante aiguë avec menace d'ischémie d'un membre : la solution est administrée en perfusion dans le thrombus, localement par cathéter. La voie IV ne doit pas être utilisée.
Surveillance thérapeutique pendant le traitement par THERASOLV : avant, pendant et après
Avant le traitement thrombolytique, les analyses de laboratoire suivantes sont indiquées :
- temps de thrombine (TT),
- temps de céphaline activée (TCA),
- temps de Quick (TQ),
- hématocrite,
- numération plaquettaire.
Si un traitement par l'héparine est utilisé, il doit être interrompu (sauf si le patient est sous hémodialyse) et le TT ou le TCA doivent être inférieurs à 2 fois la valeur de référence normale avant de débuter le traitement thrombolytique.
La surveillance thérapeutique repose sur les taux de fibrinogène circulant et des produits de dégradation du fibrinogène.
Une fois le traitement fibrinolytique terminé, un traitement anticoagulant adapté doit être envisagé, sous réserve que le TT ou le TCA soit inférieur à 2 fois la valeur de référence normale.
Identité administrative
- Liste I
- Médicament réservé à l'usage hospitalier
- THERASOLV 100 000 UI poudre pour solution injectable pour perfusion, flacon unitaire, CIP 3400955067535
- THERASOLV 250 000 UI poudre pour solution injectable pour perfusion, flacon unitaire, CIP 3400955067528
- THERASOLV 500 000 UI poudre pour solution injectable pour perfusion, flacon unitaire, CIP 3400955067511
- Agrément aux collectivités - cf. Encadré 1 (Journal officiel du 27 mars 2020 - texte 15)
- Laboratoire Theradial
Encadré 1 - Périmètre de prise en charge de THERASOLV
Lyse des caillots sanguins uniquement dans les cas suivants :
|
Pour aller plus loin
Avis de la Commission de la Transparence - THERASOLV (HAS, 5 février 2020)
Pour aller plus loin
Consultez les monographies VIDAL
Consultez les VIDAL Recos
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 4 minutes
4 minutes Ajouter un commentaire
Ajouter un commentaire
.jpg)

.jpg)




Commentaires
Cliquez ici pour revenir à l'accueil.